Sebbene ogni atomo sia costituito da particelle di dimensioni diverse, la maggior parte dello spazio, o volume, di ciascun atomo è costituito dalla sua nuvola di elettroni. Tuttavia, tra le tre molecole presenti, i neutroni sono il più grande e il nucleo dell'atomo costituisce il 99,9 percento della sua massa totale.
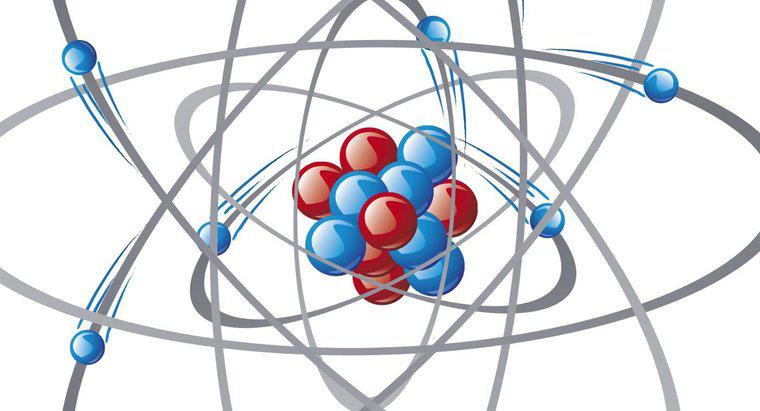
La struttura di base di ogni atomo include un nucleo fatto di protoni e neutroni e una serie di piccoli elettroni che orbitano intorno ad esso in uno spazio chiamato nuvola di elettroni. L'unica eccezione a questa struttura è l'atomo di idrogeno, che non contiene neutroni.
Gli atomi, come le particelle che formano, contengono più spazio vuoto della massa poiché la carica positiva dei protoni e la carica negativa degli elettroni si respingono l'un l'altro. Questo crea ciò che gli scienziati definiscono una "nuvola di elettroni" che circonda il nucleo di ciascun atomo. In termini di volume, la nuvola di elettroni costituisce la maggioranza dello "spazio" di ciascun atomo. Un'illustrazione comune di questo spazio indica che se il nucleo di un atomo aveva le dimensioni di un marmo, allora il bordo esterno della nuvola di elettroni sarebbe distante più di 100 iarde o un campo di calcio.
Tuttavia, nonostante il fatto che la maggior parte dello spazio di ogni atomo contenga i suoi elettroni, la maggior parte della sua massa, il 99,9 percento, si trova nel nucleo. La massa del nucleo di un atomo è divisa quasi in modo uniforme tra protoni e neutroni, sebbene i neutroni siano leggermente più grandi. La massa di un elettrone, al contrario, è pari a 1/1836 di un protone.