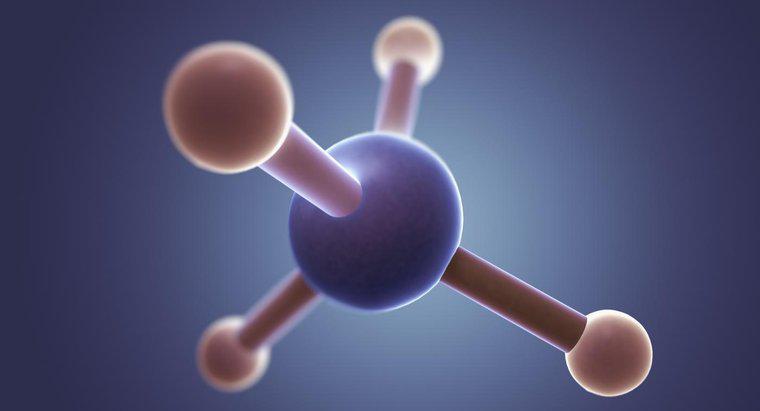
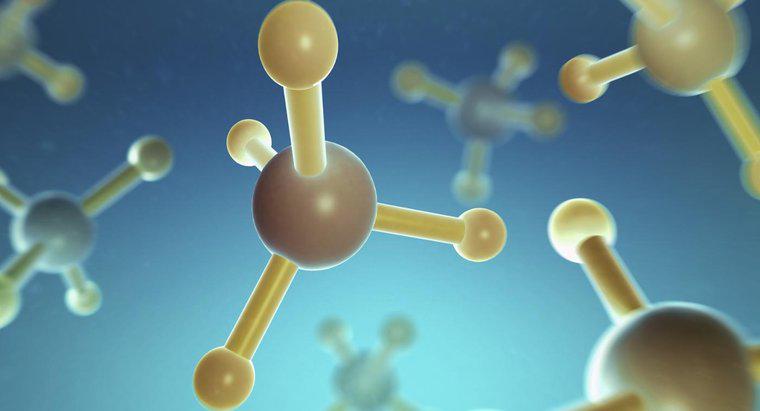
La struttura del metano, CH4, molecola mostra singoli legami covalenti. Il legame covalente implica la condivisione di elettroni. Nella molecola di metano, i quattro atomi di idrogeno condividono un elettrone ciascuno con l'atomo di carbonio.
Alcune proprietà dei legami covalenti sono che tendono a verificarsi tra due atomi non metallici, hanno punti di ebollizione e di fusione bassi e bassa polarità. A temperatura ambiente, queste molecole covalenti sono sia gassose che liquide. Ad esempio, il metano è un gas.
Al contrario, i legami ionici tendono ad essere presenti nei composti solidi. I legami ionici si verificano tra un metallo e un non-metallo. Alcune caratteristiche dei legami ionici nei composti sono che presentano punti di fusione e di ebollizione elevati.