Il legame idrogeno è una forza di attrazione tra un idrogeno leggermente positivo di una molecola in una regione leggermente negativa di un'altra molecola. Un legame idrogeno individuale non è molto forte, ma in gran numero, legami idrogeno può rappresentare una sostanziale forza di attrazione all'interno di una sostanza.
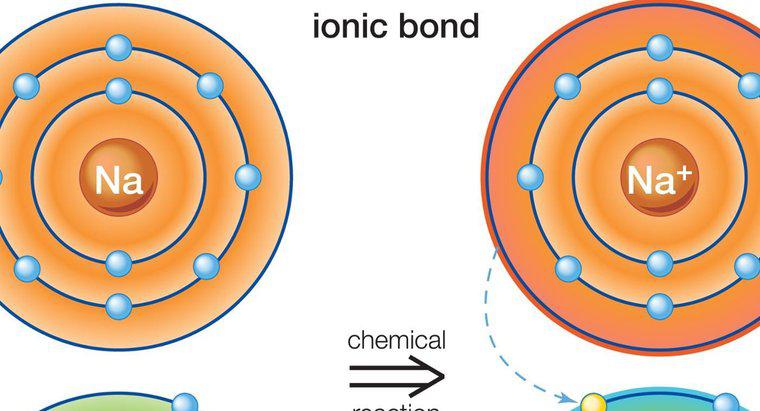
In alcuni composti contenenti idrogeno, gli elettroni sono condivisi tra gli atomi del composto. Alcuni atomi nel composto attraggono gli elettroni più fortemente dell'idrogeno; quindi, gli elettroni trascorrono più tempo intorno agli atomi che li attraggono di più. Ciò fa sì che le regioni dell'idrogeno di una molecola abbiano cariche leggermente positive e altre aree abbiano cariche leggermente negative. Le aree di idrogeno leggermente positive su una molecola attraggono le regioni leggermente negative su un'altra molecola, formando legami a idrogeno. Composti come l'acqua che contiene legami idrogeno tendono ad avere punti di ebollizione più alti e sono più spessi o più viscosi del previsto.