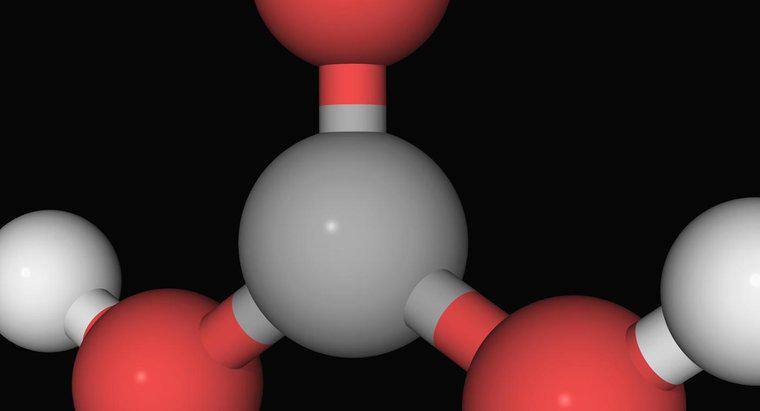
L'ammoniaca, un composto gassoso di un atomo di azoto legato a tre atomi di idrogeno, non è una base forte. È una base più debole che generalmente deve reagire con l'acqua prima che reagisca con un acido. Prima neutralizza gli acidi in una soluzione, reagisce con l'acqua per formare ioni di ammonio e idrossido. L'ammonio è uno ione positivo di un azoto e quattro atomi di idrogeno, ed è un acido debole.
Tutte le basi funzionano accettando gli ioni di idrogeno, che sono solo protoni nudi. Questo neutralizza gli acidi, poiché gli acidi agiscono rilasciando ioni di idrogeno per reagire con altri materiali. Le basi reagiscono con questi ioni in modo più potente rispetto ad altri materiali, e quindi possono proteggere questi altri materiali dagli acidi. Tuttavia, le basi stesse possono essere corrosive.
Le basi più forti, come l'idrossido di sodio, agiscono dissociando i loro ioni idrossido in soluzione. Gli ioni idrossido reagiscono molto fortemente con gli ioni idrogeno per formare acqua. Gli altri componenti degli acidi e delle basi si associano spesso come sali. Tuttavia, l'ammoniaca non contiene ioni idrossido. Deve prima reagire con l'acqua per generarli. Non solo fa un passo avanti prima di neutralizzare gli acidi, è parzialmente neutralizzato dalla creazione di ammonio, un acido più debole.