La carica complessiva o netta di qualsiasi composto ionico deve essere uguale a zero. Sebbene gli ioni stessi siano sia positivi (cationici) che negativi (anioni) per definizione, l'unico modo in cui possono legarsi insieme e formare un composto è cercando una carica opposta.
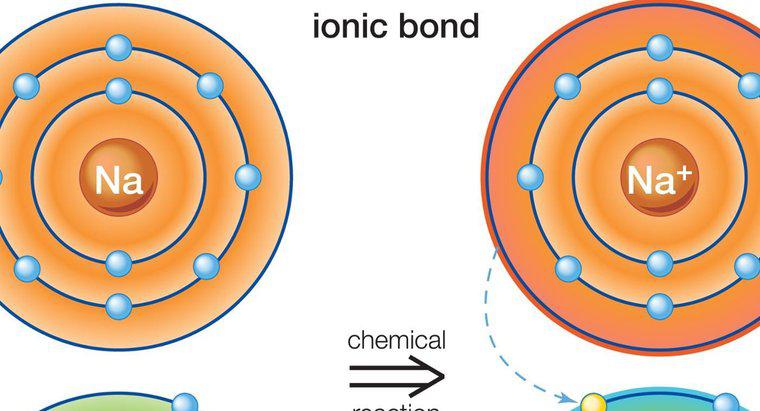
Un composto ionico in chimica si riferisce a qualsiasi composto chimico in cui gli ioni sono tenuti insieme, o legati, attraverso legami ionici. I legami ionici, per definizione, sono attrazioni elettrostatiche tra due ioni con carica opposta. In altre parole, un legame ionico può formarsi solo tra un catione e un anione.
Sebbene non vi sia un limite al numero di ioni contenuti in un composto ionico, affinché il composto rimanga intero, la carica netta deve essere uguale a zero. Pertanto, ci deve essere un numero uguale di cationi e anioni all'interno del composto completato.
Un esempio popolare e comune di un composto ionico che mostra questo principio è il sale da cucina o il cloruro di sodio, che ha la formula chimica NaCl. La formazione di sale da cucina è il risultato di un legame ionico tra un catione di sodio, Na + e un anione di cloro, Cl-. La struttura di ogni ione è diversa da un atomo dello stesso elemento (Na o Cl) che detiene una carica neutra a causa di un numero uguale di protoni ed elettroni. È solo una volta che ogni atomo diventa uno ione che è in grado di legarsi con l'altro atomo e creare un composto ionico.