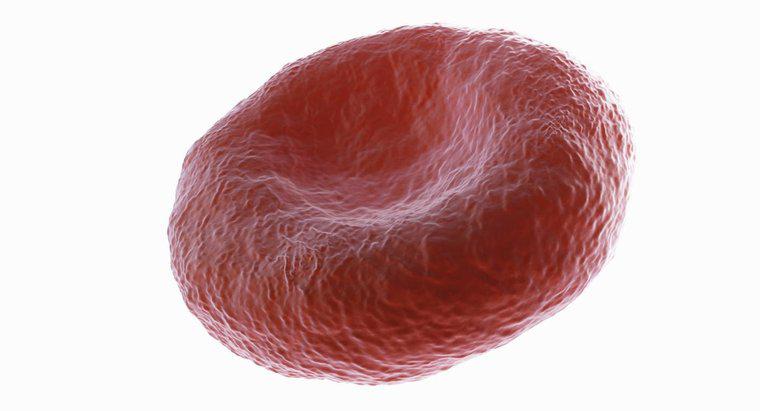
Quando i globuli rossi vengono posti in acqua distillata, che è ipotonica rispetto alla soluzione contenuta all'interno delle membrane delle cellule, l'acqua distillata si diffonderà nei globuli rossi e li farà scoppiare. Posizionare globuli rossi in qualsiasi soluzione che contenga un grado minore di soluto rispetto a quello della soluzione all'interno delle cellule farà sì che l'acqua si diffonda in essi. Poiché l'acqua distillata contiene una concentrazione zero di soluto, si diffonderà prevedibilmente in un globulo rosso nel tentativo di equalizzare la pressione osmotica su entrambi i lati della membrana cellulare.
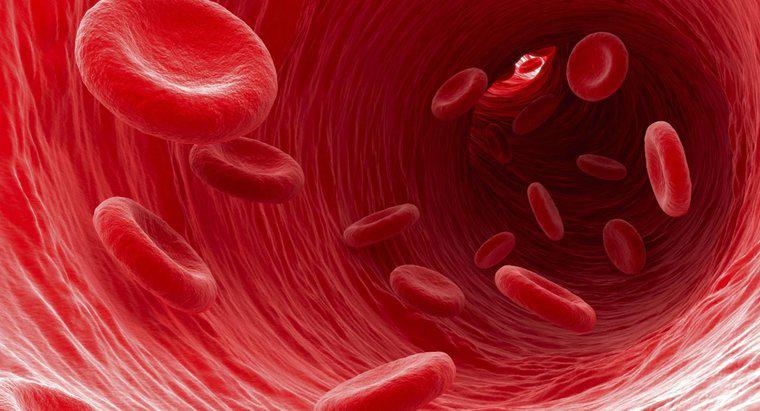
In un organismo sano, i globuli rossi sono in grado di mantenere la loro forma e non si espandono né scoppiano nel flusso sanguigno, perché la pressione osmotica all'interno della cellula è uguale alla pressione osmotica del siero del sangue che lo circonda. Questo equilibrio di pressione osmotica viene definito come isotonicità. Se il siero nel sangue dovesse contenere una minore concentrazione di soluto rispetto alla soluzione all'interno dei globuli rossi, ciò renderebbe ipotonico il siero. L'ineguale pressione osmotica indurrebbe quindi la porzione di acqua del siero del sangue a diffondersi nei globuli rossi, facendoli gonfiare.