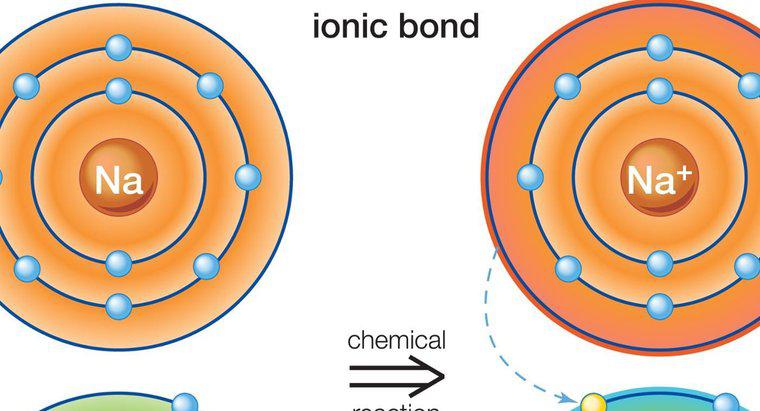
I composti ionici sono elettricamente neutri perché le cariche dei cationi e degli anioni che compongono il composto si annullano a vicenda. Nel caso del sale, ad esempio, il sodio ha una carica positiva e il cloruro ha una carica negativa. Insieme, neutralizzano il composto.
I composti ionici sono costituiti da atomi o molecole caricati positivamente e negativamente. Quelli con carica positiva sono chiamati cationi, mentre quelli con carica negativa sono chiamati anioni. I due sono attratti l'un l'altro a causa delle loro cariche opposte. Cationi e anioni possono attrarre più di una molecola del tipo opposto, creando una molecola più lunga tenuta insieme da legami ionici.
Il calcio cloruro è un altro esempio di un composto ionico, con il calcio positivo che cancella il cloruro negativo. Il bromuro di ferro fa lo stesso, con la carica positiva del ferro che cancella la carica negativa dal bromuro. Questa neutralità elettrica aiuta a mantenere stabile il composto, rendendo più facile il lavoro e molto meno volatile rispetto agli ioni instabili.
La maggior parte dei composti ionici sono solidi con punti di fusione elevati. Sono spesso formati da un elemento metallico e uno non metallico. I composti ottenuti da due non metalli sono spesso composti con legame covalente.